Sundejme si růžové brýle a přiznejme si, že oblast fitness a kulturistiky je jedním ze sportů, kde četnost užívání zakázaných látek patří mezi nejvyšší a zdaleka se nevztahuje pouze na ty, které jejich tělo živí a kde jsou tyto látky prakticky podmínkou úspěchu. Ženy v tomto ohledu nejsou žádnou výjimkou. Podle šetření Striegela (2006) u pravidelných návštěvníků posiloven může mít zkušenost s anabolickými steroidy téměř 20 % mužů 4 % žen.
Co se v dnešním článku dozvíme?
- Jak se dělí zakázané látky podle Světové dopingové agentury WADA.
- Jaké jsou pozitivní a negativní účinky anabolických steroidů.
- Může být rychlý nárůst svalů zapříčiněn kombinací kreatinu s proteinem?
- Proč se mužům při užívání anabolik zvětšuje prsní žláza a hojně se objevuje akné.
- Jak se podepíše užívání anabolik na ženském těle.
- Že užívání anabolických látek v duchu fair‑play a zdraví není to pravé ořechové.
V dnešní době může anabolické steroidy užívat téměř kdokoliv a je velmi pravděpodobné, že s někým takovým se denně setkáváte ve fitku. Téměř vždy, když někoho podezřele velkého, dokonce většího než my sami, uvidíme v posilovně, nám vyvstane na mysli otázka: "Jak je možné, že je větší než já? Má to ten borec čistě, nebo na něčem jede?" Jak asi tušíte, jen na samotné velikosti nezáleží, neboť ta může být vyjádřena nejen svalovou hmotu, ale často i přebytečnou vodou a tukem.
Těžko se budete velkého neznámého dotazovat na jeho tělesnou hmotnost, výšku a procento tělesného tuku, abyste si potají vypočítali jeho FFMI (index beztukové hmotnosti těla). Existují tedy jiné, poměrně přesné tělesné znaky toho, že jedinec "něco bere“? Můžeme říci že ano, dokonce jsou vědecky doložitelné a dnešní článek vám tyto příznaky přiblíží.
Jak zakázané látky dělí Světová dopingová agentura WADA?
Androgenní anabolické steroidy (AAS) jsou skupinou látek, mezi které se řadí mužský pohlavní hormon testosteron a jemu podobné uměle vyráběné hormony s podobnými účinky. AAS však nejsou jedinou skupinou zakázaných látek užívaných ve sportu. Světová dopingová agentura rozděluje zakázané látky do deseti skupin (S0–S9). Konkrétně AAS se řadí do skupiny S1.

Anabolické steroidy se běžně užívají v medicíně a bohužel i ve sportu
Problematiku AAS nelze vnímat úplně černobíle a zdaleka nelze říci, že jejich užívání s sebou přináší pouze negativa. AAS jsou totiž využívány i v medicíně jako podpůrná léčba při chorobách s úbytkem svalové hmoty. Mezi tyto choroby řadíme HIV, chronické choroby jater a ledvin, nebo pooperační stavy (Basaria, 2001).
Aplikace AAS ve sportu přináší jak kýžené žádoucí účinky, kvůli kterým jsou užívány, tak na druhou stranu i negativní (nežádoucí) účinky, kterým musí jejich uživatelé čelit. V tomto článku se však zaměříme pouze na ty účinky, které jsou viditelné a "bijí" do očí téměř na první pohled. Pokud si pro potřeby tohoto článku rozdělíme viditelné účinky steroidů a dalších látek na pozitivní, to znamená na ty, které jsou hlavním důvodem jejich užívání nebo jsou příjemným bonusem, a na negativní, které se v menší či větší míře vyskytují, pak můžeme dostat následující rozdělení.
Pozitivní známky užívání anabolických steroidů
- Rychlý nárůst hmotnosti
- Nezvykle vyvinutá oblast ramen, trapézů a horní oblasti prsních svalů
A nyní ty o poznání méně příjemné negativní známky
- Gynekomastie (zvětšená prsní žlázy u mužů)
- Akné
- Vypouklá břicha a široký pas (týká se růstového hormonu nebo inzulinu)

10 kg kvalitní hmoty za 6 týdnů aneb Kreatin s proteinem, nebo AAS?
Anabolické steroidy zvyšují syntézu svalových bílkovin, což je pokládáno za hlavní mechanismus jejich účinku. Dalším, méně často zmiňovaným mechanismem, který je považován za nepřímý, je schopnost testosteronu a jeho derivátů vázat se na receptory hormonu kortizolu a blokovat tak jeho navázání se na ně. Proto můžeme říci, že vysoké dávky testosteronu a jeho derivátů poněkud snižují katabolické působení stresového hormonu kortizolu (Basaria, 2001; Sheffield‑Moore et al., 1999).
Pokud budeme vycházet čistě z vědeckých pramenů, tak se podle jednoho anonymního průzkumu mezi uživateli AAS dostaneme k popsání charakteristického steroidového cyklu (Perry et al., 2005).
Jaké jsou hlavní charakteristiky typického steroidového cyklu?
- Průměrná délka cyklu užívání je 5–10 týdnů.
- V průměru se současně užívají tři různé látky s anabolickým účinkem (tzv. stacking). Z více látek to prostě více roste a ve svém působení se navzájem podporují.
- Celkový nárůst hmotnosti se za období jedné kúry může lišit, nicméně se může klidně vyšplhat až k 10 kg hmoty. O tom, jak kvalitní tato hmota bude, rozhodují konkrétní užívané látky, trénink, strava a genetické predispozice.
Čím je tedy tento rychlý nárůst hmotnosti způsoben?
Hlavním důvodem rychlého nárůstu hmotnosti je celková dávka AAS a druh steroidu. Pokud vezmeme v úvahu průměrnou denní produkci testosteronu mladého muže, která nejčastěji spadá do rozmezí 3–7 mg, a srovnáme ji s kúrami, které zcela běžně obsahují stovky miligramů účinných látek týdně, je jasné, že tento "signál" dává svalovým buňkám obrovský impuls k růstu (Vierhapper, 1997).
Téměř každý naturální cvičenec za první 2–3 roky produktivního tréninku nabere podstatnou většinu svých celoživotních svalových přírůstků. Pokud po uplynutí těchto plodných začátků zčistajasna začne růst téměř trénink od tréninku, můžete si být jisti, že za tímto rychlým nárůstem hmotnosti nestojí nalezení magického tréninkového splitu nebo kombinace proteinu, kreatinu a rychlých cukrů po tréninku, jak se vám možná bude chtít namluvit. Za takto rychlý nárůst v kvalitní tělesné hmotnosti jsou zodpovědné AAS!
Ramena jako dělové koule a trapézy sovětského vzpěrače
Dalším typickým rysem uživatelů anabolických steroidů je nezvykle esteticky působící oblast ramen, horních trapézů a prsních svalů. Proč tomu tak je? Tato skutečnost má co dočinění s koncentrací androgenních receptorů, na které se váže testosteron a jemu podobné látky. Poté, co se látka naváže na tento receptor, je aktivována kaskáda dějů uvnitř buňky vedoucí ke zvýšené syntéze svalových bílkovin. Právě v této oblasti je koncentrace receptorů nejvyšší, a proto tyto partie nejlépe reagují na podávání AAS.
Hezky kulatá ramena a vyvážený rozvoj všech tří hlav deltových svalů propůjčující této partii jakýsi 3D vzhled, který je naturální cestou velice těžké dosáhnout a můžeme je vidět pouze u jedinců s přirozeně vyšší hladinou testosteronu. Důležitou roli zde může hrát i technika provedení cviků.
Podobně to platí i pro oblast horních prsou, kterou je těžké správně odizolovat a stimulovat cvičením k růstu. Vysoká hustota androgenních receptorů a administrace AAS však tento problém elegantně obchází. Partie jako lýtka mají naopak hustotu androgenních receptorů typicky velmi nízkou, tudíž ani velké dávky AAS nijak významně tuto partii nemusí zvětšit.
Vysoký růstový potenciál ramen může být evolučního charakteru!
Někteří autoři v této vysoké koncentraci androgenních receptorů typickou pro oblast ramen vidí i důvod evoluční. Široká vyvinutá ramena jsou vždy vidět z velké vzdálenosti, a tak jsou jistým rysem, který může okolí napovědět, že jedinec disponující takovými rameny má vyšší hladinu testosteronu, tudíž není radno si s ním nic "začínat" a pouštět se do souboje. Podobně pozitivní roli tento efekt mohl hrát i při vybírání partnerky a možnosti rozšíření svých genů prostřednictvím zplození potomka. Ženy široká ramena většinou podvědomě vnímají a mohou v nich vyvolávat pocit bezpečí a jistotu kvalitních genů pro své potomstvo.

Gynekomastie aneb Prsa nemají jen ženy
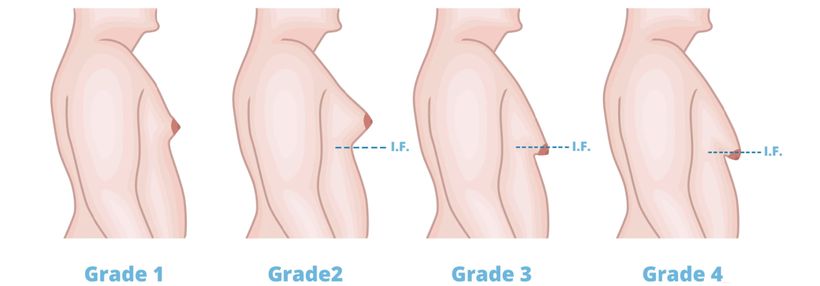
Od pozitivních projevů anabolik na vzhled se nyní dostáváme již k těm méně příjemným. Co si pod pojmem gynekomastie máme vlastně představit? Gynekomastie je nežádoucí účinek AAS projevující se zvětšením tkáně prsní žlázy v okolí prsních bradavek.
Neměla by se zvětšit prsní žláza jen v případě užívání estrogenu?
Jak je možné, že právě s tímto může být při užívání anabolik problém? Vysvětlení je poměrně jednoduché. Mužský pohlavní hormon je totiž velmi podobný ženskému pohlavnímu hormonu estrogenu. Jsou si dokonce tak podobné, že z testosteronu estrogen může přímo vznikat (Shoham, 1996).
Za tuto přeměnu jsou zodpovědné enzymy zvané aromatázy.
I v mužském organismu se tedy z testosteronu zcela běžně syntetizuje určité množství estrogenu. O tom, kolik vznikne estrogenu, rozhoduje aktivita a množství těchto aromatáz a v neposlední řadě však také množství testosteronu v organismu. Čím více dodaného testosteronu prostřednictvím kúry, tím teoreticky větší množství vzniklého estrogenu, který může zvětšovat prsní žlázu a gynekomastie je na světě(Simpson, 2001).
Profi kulturisté však umějí vznik gynekomastie minimalizovat látkami blokující receptory pro estrogeny
Významnou roli zde mohou hrát i individuální rozdíly v aktivitě tohoto enzymu. Možná se ptáte, proč je gynekomastie u top kulturistů poměrně minoritní záležitostí? Profi kulturisté si působení estrogenu mohou ošetřit podáváním látek blokující receptory pro estrogeny, tudíž prsní tkáň na zvýšenou hladinu estrogenů nemusí reagovat (Aguirre, 2015; Goodsell, 2002).
Proč se gynekomastie objevuje i u mužů s vysokým podílem tuku bez užívání anabolik?
Jak si však někteří z nás všimli, gynekomastie se nevyhýbá ani mužům s nadváhou a obezitou, kteří anabolika neužívají. Enzym aromatáza se nachází i v tukové tkáni. Pokud je v organismu více tukové tkáně, zvyšuje se i celkové množství aromatázy v organismu a ta přeměňuje větší množství testosteronu na estrogen, jehož zvýšená hladina u citlivějších jedinců může způsobovat gynekomastii (Johnson & Murad, 2009).
Akné se objevuje ve spojitosti s vyšší hladinou testosteronu
Akné může být dalším projevem užívání anabolických steroidů. Čím je akné ve spojitosti s působením anabolik způsobeno? Akné jako takové je zánětlivé onemocnění vlasového folikulu s přídatnou mazovou žlázou (Čadová, 2006).
Aktivita mazové žlázy je, mimo jiné, řízena hormonálně a mezi hormony ovlivňující její činnost se řadí i androgeny, kam patří nám dobře známý testosteron. Bylo prokázáno, že zvýšené hladiny androgenů mohou zvyšovat produkci mazu. Zvýšená produkce mazu zvyšuje riziko zanícení folikulu, což vede k viditelným projevům akné na kůži. Při užívání anabolik se může zvyšovat tvorba mazu a u náchylných jedinců dochází k projevům akné typicky na obličeji, prsou a horní oblasti zad (Toyoda & Morohashi, 2001).
Vypouklá břicha a široký pas
Poslední výrazně viditelný nežádoucí účinek způsobený užíváním podpůrných látek představují pro dnešní kulturistickou scénu tak typická vypouklá břicha některých kulturistů. Na začátek je nutné uvést, že tento nežádoucí účinek s největší pravděpodobností není způsoben užíváním AAS. Je však také zřejmě způsoben působením hormonů, v tomto případě hormonů peptidové povahy, a to:
- Růstový hormon (GH – growth hormone), (dle WADA skupina S2)
- Inzulin (dle WADA skupina S4)

Užívání růstového hormonu může způsobovat růst orgánů v břišní dutině a rozšiřovat břišní stěnu
Růstový hormon je látka tělu vlastní, která, jak už název napovídá, zapříčiňuje růst, a tak nás nepřekvapí, že k nejvyšší sekreci dochází v dětství a s tím, jak člověk stárne, se jeho sekrece snižuje. Pro nás může být zajímavé to, že trénink s vysokým podílem anaerobní zátěže může jeho sekreci zvyšovat. Tato množství však nelze srovnávat s dávkami běžně (zne)užívanými kulturisty (Godfrey, 2003).
Vysoké dávky růstového hormonu mohou způsobovat růst orgánů v břišní dutině, a tak celkově rozšiřovat břišní stěnu. U jedinců s patologicky zvýšenou tvorbou růstového hormonu v dospělosti jsou pozorovány i změny rysů v obličeji, zejména zvětšení nadočnicových oblouků, brady, čelistí, nebo nosu. I u některých kulturistů jsou tyto změny obličejových rysů více či méně patrné (Rokyta, 2008).
Na rozvoji širokého pasu se může podílet i zvýšené zadržování tekutin kvůli užívání růstového hormonu
Jiným možným vysvětlením je zvýšené ukládání tuku v břišní dutině působením růstového hormonu. Toto tvrzení však zřejmě není pravdivé, neboť jedna ze studií prokázala pravý opak (Hong et al., 2011). K zhoršenému vzhledu širokého pasu může přispívat i zvýšené zadržování tekutin způsobené užíváním růstového hormonu (Holt & Sönksen, 2008).
Nebo za rozšířením břišní stěny může být inzulín?
Druhým kandidátem je hormon inzulin. Nezodpovědné užívání inzulinu nebo jeho dlouhodobě nadměrné vylučování v organismu může vést k inzulinové rezistenci. Inzulinová rezistence je spojována s vyšším množstvím břišního (viscerálního) tuku.
Můžou být vypouklá břicha kulturistů následkem zvýšeného ukládání tuku do břišní dutiny? Otázkou zůstává, zda inzulinová rezistence zvyšuje ukládání tuku do břišní dutiny, nebo naopak, zda zvýšené ukládání viscerálního tuku zhoršuje inzulinovou rezistenci. Jinými slovy, zda bylo dříve slepice, či vejce (Pouliot et al., 1992).
Za vypouklým břichem a širokým pasem bude spíše kombinace užívaných látek
Posledním možným vysvětlením je jednoduše současné podávání vysokých dávek inzulinu i růstového hormonu a tím i jejich společný podíl na tomto nežádoucím účinku. Za normálních podmínek ve zdravém lidském organismu se totiž vysoké hladiny růstového hormonu i inzulinu současně nevyskytují. Kulturisté jsou v tomto ohledu tak trochu "pokusnými králíky." Jsou to právě oni, kteří ve svých kúrách kombinují takové množství a druhy hormonů, které by si nikde na světě žádný vědec nemohl ve svém výzkumu dovolit někomu podat.

Jak se podepíše užívání anabolických steroidů na ženách?
Jak jsme si zmínili na začátku, ani u žen není užívání AAS raritní záležitostí. Průměrná žena má denní produkci testosteronu v množství 0,1–0,4 mg, což je zhruba 20krát méně než u mužů. Proto ženám stačí užívat mnohem menší dávky než mužům. Poměr “žádoucích” a nežádoucích účinků je dán množstvím užívaných látek, délkou užívání a genetikou (Burger, 2002).
Podobně jako u mužů, tak i u žen na podávání AAS nejlépe reaguje oblast ramen a trapézů. S prodlužující se délkou užívání AAS se žena vystavuje zvyšujícímu se riziku výskytu mnoha nežádoucích účinků, které jsou souhrnně pojmenovány jako tzv. maskulinizace a virilizace (Rokyta, 2008).
Co se skrývá za tajemným pojmenováním maskulinizace a virilizace?
- Nezvratné změny hlasu
- Nepravidelnost menstruačního cyklu, případně jeho vymizení
- Snížení tvorby vlastních pohlavních hormonů
- Zmenšení prsou
- Růst vousů
- Výrazný nárůst ochlupení
Brát, nebo nebrat? – To je otázka
Užívání AAS a dalších zakázaných látek v sobě nese dvě roviny – fair play a zdraví. V rámci soutěžení a zachování duchu fair play by mělo být užívání podpůrných látek tvrdě odsuzováno v každém sportu. Otázkou však zůstává, zda dnešní doba a všeobecný společenský požadavek na maximální výkon za všech okolností prakticky nenutí mnohé sportovce tyto prostředky užívat.
Pokud někdo nemá soutěžní ambice, logicky se ho rovina fair play až tolik netýká. Mnohem palčivější rovina však bude ta zdravotní. Ve svém okolí znám několik uživatelů AAS. Mohu vám říci, že je to tak trochu pomíjivá sláva. Aplikace AAS vám dovolí zažít zvýšený zájem a obdivné pohledy mnohých návštěvníků posiloven. O to bolestnější okamžiky však nastávají po vysazení. Ztráta téměř všech svalových přírůstků, vyprchání zájmu o cvičení nebo mnohé nežádoucí účinky popsané v článku, ale i jiné, méně viditelné, a o to možná nebezpečnější (deprese, poškození orgánů, vyšší riziko vzniku některých nádorů). Já osobně bych užívání podpůrných prostředků rozhodně nedoporučil. Ty, kteří se pro užívání rozhodli nebo rozhodnou, však neodsuzuji.















